Ventajas de los estudios de perfiles de disolución como prueba de intercambiabilidad
Los estudios de perfiles de disolución, como sustitutos de pruebas de bioequivalencia, son una alternativa para que la población pueda tener acceso directo a algunos medicamentos de calidad a un menor precio.
Por: Q.F.B. Yadira Hernández Ruiz y Dr. en Ciencias Melby Dessiré Mendoza Aguilar
De acuerdo con la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), existen tres tipos de pruebas que pueden realizarse a los productos que pretenden ser registrados como medicamentos genéricos:
- Prueba A: Buenas Prácticas de Fabricación
- Prueba B: perfiles de disolución
- Prueba C: estudios de bioequivalencia
Para la Prueba A únicamente es necesario presentar la Licencia Sanitaria del Laboratorio fabricante y el Certificado de Buenas Prácticas de Fabricación del medicamento. En el caso de productos de inhalación en suspensión, la Prueba A incluye pruebas de determinación de tamaño de partícula mediante el método de cascada, que puede realizar directamente el fabricante por tratarse de una prueba de control de calidad.
La Prueba B puede ser solicitada en uno o tres medios de disolución, y será indispensable calcular el valor del factor de similitud (f2) con respecto al medicamento de referencia. Este estudio debe ser realizado por una Unidad Analítica de Perfiles de Disolución autorizada por Cofepris.
En el caso de la Prueba C (estudios de bioequivalencia), debido a que existen subcategorías que dependen de la naturaleza del fármaco, los requisitos solicitados para llevar a cabo este tipo de estudios pueden variar. Los estudios de bioequivalencia pueden realizarse con sujetos sanos o pacientes, y ser estudios de farmacocinética, farmacodinamia o pruebas especiales. El precio de un estudio de bioequivalencia se determina según la naturaleza de las pruebas a realizar.
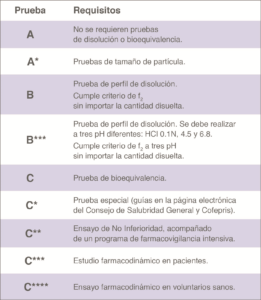
Tipos de pruebas para demostrar la intercambiabilidad de medicamentos genéricos ante Cofepris.
A diferencia de los estudios de bioequivalencia, los estudios de perfiles de disolución suelen ser menos costosos, pues no incluyen pruebas que involucren a voluntarios ni requieren la participación de la Unidad Clínica y la Unidad Analítica de Intercambiabilidad. En los estudios de perfiles de disolución solo participa un Tercero Autorizado por Cofepris.
Por ejemplo, un estudio de bioequivalencia de paracetamol tiene un costo aproximado, en México, de 1.5 millones de pesos y una duración de 4 meses, mientras que un estudio de perfiles de disolución de un mes de duración, para el mismo medicamento, ronda los 120 mil pesos.
Desde 2008 a 2017 se ha incrementado de 32 a 215 el número de medicamentos que deben demostrar intercambiabilidad a través de un estudio de perfiles de disolución –según lo indica el acuerdo que determina el tipo de prueba para demostrar la intercambiabilidad de medicamentos genéricos–, por lo que se espera que esta tendencia continúe.
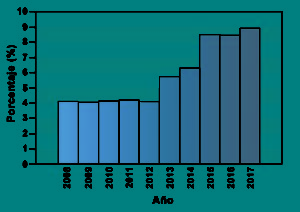
Aumento de solicitudes de Pruebas tipo B, expresado como porcentaje de medicamentos que requieren este tipo de pruebas como función del tiempo.
Además de disminuir costos y tiempo, los estudios de perfiles de disolución evitan la exposición de sujetos a fármacos que causan efectos adversos, posibles o bien documentados, desde leves hasta severos.
De acuerdo con la European Medicine Agency (EMA), un medicamento se considera altamente soluble si la dosis más alta del fármaco se disuelve completamente en 250 mL de soluciones amortiguadoras en el intervalo de pH 1.0 a 6.8 a 37 ± 1°C.
Alcance de los estudios de perfiles de disolución
Más allá de su uso para comprobar intercambiabilidad, los estudios de perfiles de disolución tienen muchas otras aplicaciones: con ellos se puede verificar la consistencia entre los lotes de producción de un medicamento, estudiar si existen cambios debidos a modificaciones en la formulación, e incluso comprobar si las dosis bajas de un medicamento aplican para exención por linealidad de dosis.
A nivel internacional, los estudios de perfiles de disolución se han utilizado como mecanismos para demostrar la bioequivalencia, comparando las propiedades de solubilidad y permeabilidad, de dos diferentes formulaciones orales de liberación inmediata con un mismo principio activo, para así evitar realizar estudios de biodisponibilidad–un procedimiento conocido como Bioexención.
Bioexenciones
A diferencia de las exenciones por linealidad de dosis, las bioexenciones se basan en el Sistema de Clasificación Biofarmacéutica (SCB), que agrupa a los medicamentos en cuatro clases de acuerdo a su solubilidad y permeabilidad, y aplica a las formas farmacéuticas sólidas de liberación inmediata.
Para que un medicamento genérico pueda ser candidato a una bioexención, el fármaco debe pertenecer a las clases I o III del SCB, según FDA y EMA, aunque la OMS acepta su aplicación también para fármacos clase II. Debido a sus características de bajas permeabilidad y solubilidad, los fármacos de la clase IV no se consideran elegibles para bioexenciones.
La guía de la EMA 2010 define la permeabilidad en función de la extensión de la absorción después de la administración oral; una completa absorción está relacionada generalmente con una alta permeabilidad.
En México, la aplicación de bioexenciones aumentaría el número de medicamentos genéricos que requerirían la Prueba B para demostrar intercambiabilidad, lo cual conllevaría a una disminución de su precio al público y facilitaría el acceso a estos medicamentos.

Sistema de Clasificación Biofarmacéutica.
En LEI (Laboratorios de Especialidades Inmunológicas), con el amplio compromiso con la industria farmacéutica que nos caracteriza y como apoyo a la autoridad sanitaria, hemos ingresado al campo de los estudios de perfiles de disolución. Con nuestra amplia experiencia y calidad reconocida a nivel nacional, nos encontramos autorizados como Unidad Analítica de Perfiles de Disolución, con lo cual buscamos poner a disposición de Cofepris y de las empresas de medicamentos genéricos nuestras instalaciones y personal capacitado.




 CONTROL DE CALIDAD
CONTROL DE CALIDAD ESTUDIOS ESPECIALIZADOS
ESTUDIOS ESPECIALIZADOS DIVTTma
DIVTTma PROTOCOLOS DE ESTABILIDAD
PROTOCOLOS DE ESTABILIDAD INVESTIGACIÓN Y DESARROLLO
INVESTIGACIÓN Y DESARROLLO SERVICIOS VETERINARIOS
SERVICIOS VETERINARIOS CURSOS Y EVENTOS
CURSOS Y EVENTOS MICROBIOLOGÍA
MICROBIOLOGÍA


